- ЗЂВМЪБМфЃК2008-11-24 08:11:00
- ЗЂВМепЃКЮсАЎ
- ЮЂаХКХЃКwuaiyazhu.
- фЏРРСПЃК
- TagsЃК
-
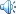 ЙЋИцЃК
ЙЋИцЃК
ЛЏКЯМлЃЈ2ПЮЪБЃЉ

вЛ.жЊЪЖНЬбЇЕу
1.ЛЏКЯМлЕФКЌвхЁЃ
2.дЊЫиЛЏКЯМлгыЛЏбЇЪНЕФЙиЯЕЃЌФмИљОнЛЏКЯМлЪщаДЛЏбЇЪНЛђИљОнЛЏбЇЪНХаЖЯЛЏКЯМлЁЃ
Жў.жиЁЂФбЕу
1.жиЕуЃК(1)ЛЏКЯЮяжае§ИКЛЏКЯМлЕФДњЪ§КЭЮЊСуЁЃ
(2)МЧзЁГЃМћдЊЫиЕФЛЏКЯМлЁЃ
2.ФбЕуЃКЛЏКЯМлИХФюЕФНЈСЂЁЃ
Ш§.НЬбЇВНжш
(вЛ)УїШЗФПБъ
1.СЫНтЛЏКЯМлЕФИХФюМАКЌвхЃЌГѕВНШЯЪЖЛЏКЯМлЕФЪЕжЪЃЌМЧзЁГЃМћдЊЫиЕФЛЏКЯМлМАЛЏКЯМлЕФвЛАуЙцТЩЁЃ
2.СЫНтЛЏКЯМлгыЛЏбЇЪНЕФЙиЯЕЃЌЛсРћгУЛЏКЯМлддђИљОнЛЏКЯМлЪщаДЛЏбЇЪНЛђИљОнЛЏбЇЪНХаЖЯдЊЫиЕФЛЏКЯМлЁЃ
(Жў)ећЬхИажЊ
ЛЏКЯМлЪЧГѕжаЛЏбЇПЮГЬжавЊЧѓДяЕНСЫНтЫЎЦНЕФЛљДЁжЊЪЖЁЃдкДЫвдЧАЩцМАЕФгаЙиЛЏбЇЪНЃЌЮяжЪНсЙЙЕФГѕВНжЊЪЖЃЌгШЦфЪЧгаЙиРызгЛЏКЯЮяКЭЙВМлЛЏКЯЮяЕФжЊЪЖЪЧИјГіЛЏКЯМлЕФвРОнЁЃ
(Ш§)НЬбЇЙ§ГЬ
[ИДЯАв§Шы]ЃКЧАУцЮвУЧбЇЯАСЫгаЙидзгНсЙЙЕФГѕВНжЊЪЖЃЌФЧУДЃЌЪЧЪВУДОіЖЈСЫдЊЫиЛЏбЇаджЪЃП
[ЬсЮЪ]ЃКЯТУцЮвУЧПДвЛЯТЭЖгАЦЌЃЌЬжТлетаЉдЊЫиСНСНзщКЯПЩвдзщГЩФФаЉЛЏКЯЮяЃП
[ЭЖгА]ЃК |
|
[СЗЯА]ЃКаДГіЛЏбЇЪНВЂХаЖЯУПжжЛЏКЯЮяжадзгИіЪ§БШЁЃ
[змНс]ЃКРызгЛЏКЯЮяЃКNaCl MgCl2 Na2S MgS Na2O MgO
дзгИіЪ§БШЃК1:l 1:2 2:1 1:1 2:1 1:1
ЙВМлЛЏКЯЮяЃКHCl H2O H2S SO2
дзгИіЪ§БШЃК1:1 2:1 2:l 1:2
[аТПЮв§Шы]ЃКДгЩЯУцЕФСЗЯАПЩвдПДЕНдзгжЎМфаЮГЩЛЏКЯЮяЪБЦфдзгИіЪ§БШгаШЗЖЈЕФЪ§жЕЃЌШчЙћВЛЪЧетИіБШжЕФЧУДОЭВЛФмаЮГЩЮШЖЈЕФЛЏКЯЮяЁЃЖјдЊЫидзгжЎМфЯрЛЅЛЏКЯЕФИіЪ§БШгжЪЧгЩдзгЕФзюЭтВуЕчзгОіЖЈЕФЃЌвВОЭЪЧЫЕЃЌдзгЕФзюЭтВуЕчзгНсЙЙОіЖЈСЫдзгжЎМфАДвЛЖЈЪ§ФПЯрЛЅЛЏКЯЁЃЖјетИіЪ§ФПОЭБэЯжГіСЫдЊЫиЕФдгкдкаЮГЩЛЏКЯЮяЪББэЯжГіЕФвЛжжЛЏбЇаджЪЁЊЁЊЛЏКЯМлЁЃ
ЩЯвЛЦЊЮФеТЃКЕкЮхНк КЫЭтЕчзгХХВМЕФГѕВНжЊЪЖ ЃЈ2ПЮЪБЃЉ
ЯТвЛЦЊЮФеТЃКЕквЛНк ЬМЕФМИжжЕЅжЪ
БОРрИќаТ
- ТГНЬАцОХФъМЖЛЏбЇЫЕПЮИх ДжбЮЬсДП
- ГѕжаЛЏбЇЮЂПЮбЇЯАЩшМЦ
- ШМСЯЕФКЯРэРћгУгыПЊЗЂНЬбЇЩшМЦ
- жЪСПЪиКуЖЈТЩЮЂПЮЩшМЦ
- ГѕжаЛЏбЇзЈЬтИДЯАЮЂПЮЩшМЦ ЛЏбЇЭЦЖЯ...
- ЫсЕФаджЪЮЂПЮЩшМЦ
- ГѕжаЛЏбЇЮЂПЮЩшМЦ ЦјЬхЪеМЏзАжУЕФбЁ...
- ОХФъМЖЛЏбЇжаПМИДЯАМЦЛЎ
- ЛЏбЇЪЧвЛУХвдЪЕбщЮЊЛљДЁЕФПЦбЇНЬАИ...
- ЮяжЪЕФБфЛЏКЭаджЪНЬбЇЩшМЦ
- ХфжЦвЛЖЈШмжЪжЪСПЗжЪ§ЕФШмвКЕМбЇАИ...
- ШЫНЬАцГѕжаЛЏбЇЕквЛЕЅдЊВтЪдЬт
БОРрШШУХ
- ОХФъМЖКЎМйзївЕД№АИ
- 2014ФЯЗНГіАцЩчОХФъМЖПьРжКЎМйД№АИ...
- ШЫНЬАцОХФъМЖЛЏбЇНЬАИ бѕЦјЃЈЕквЛПЮ...
- ШЫНЬАцОХФъМЖЛЏбЇНЬбЇЩшМЦЕквЛЕЅдЊ...
- ЧсЫЩПьРжЙ§КЎМйД№АИ ОХФъМЖЛЏбЇ
- ЩЯКЃНЬг§ГіАцЩчГѕжаЛЏбЇ(ЛІНЬАц)
- ЛЏбЇЫЕПЮИхФЃАх
- ГѕжаЛЏбЇгХауНЬбЇЩшМЦЃКЁЖАЎЛЄЫЎзЪ...
- ОХФъМЖЛЏбЇЩЯВсЦкжаЪдОэМАД№АИ
- ЕкАЫЕЅдЊН№ЪєКЭН№ЪєВФСЯ ПЮЬт2 Н№...
- ШЫНЬАцОХФъМЖЛЏбЇНЬАИ ЮяжЪЕФБфЛЏКЭ...
- ОХФъМЖЯТбЇЦкЛЏбЇНЬбЇЙЄзїМЦЛЎ