第3课时氧气的性质
一、 氧气的性质:
1. 物理性质:通常状况下:O2是无色无味的气体、密度比空气大,不易溶于水(常温下1体积水能溶0.03体积O2)。 在一个标准大气压,―
2.化学性质:演示实验,学生观察化学实验现象
①木炭、蜡烛燃烧实验同时进行,学生进行比较(注意:木炭要干,无火焰水雾,加石灰水后振荡后能吸玻片。
② 硫磷同时做:注意与该物质在通常的空气中燃烧现象对比,写符号告知S,让学生用二氧化硫图式同化SO2,教师告知五氧化二磷书写注意点。准备氢氧化钡溶液吸收两物质。
③铁丝长螺旋进行较长时间的燃烧,告知Fe,学生自写四氧化三铁。铁丝在氧气中燃烧,若不做实验为话学;教师演示,学生观察或实验,学生在观察中思考,得出氧浓度大铁丝才燃烧,如果温度高在空气中也能燃烧,为活动教学。
四、讲述1、氧气能和许多物质发生反应,在较高的温度下还会出现燃烧现象,我们通过和其它气体比较,确认它是一种化学性质比较活泼的气体。
※从细节中进行抽象,去把握整体的总的轮廓,再从整体去看细节就会形成较完整的表象。
2.从上述实验现象,我们还可以得出哪些结论或看法或规律。
※①氧浓度大燃烧激烈。(可燃物在空气中燃烧远不如纯氧中剧烈,因为物质燃烧是与氧气反应,而空气中氧气只占其体积的1/5,与可燃物接触不如纯氧充分)②燃烧需要点燃或加热 ③通常不燃烧的物质在纯氧中也可燃
注意:铁等金属在空气中不易燃烧(不是不能)液氧中则炸)
空气中氧很少时铁也能燃烧吗?(能――陨石铁)
3.并列写出反应文字表达式,并按以下顺序呈现C、S、P、Mg、Fe、蜡烛
问题:如何记住上述反应特征?学生讨论,交流(把客体组合)归纳。
注意其中分类方法:从而引出化合反应,氧化反应的概念,(注意:氧化反应的表述,不需强调是氧,而不是氧气,要含混一点)也可以提出从生成物的种类多少和从参加反应的物质和氧反应这共同特点来分类。在深入思考的基础上的识记,实质上就是知识的运用,借助运用知识不断学习新知识。
五、学生根据氧气的性质说出它的用途,越多越好 教师当场评价。
六、对照课文、学生回顾学习过程中的问题,演练反思,评价、调节、提出问题(适当练习)
板书设计:也可加文字
氧气能与 多种物质 在高温下 发生剧烈化学反应
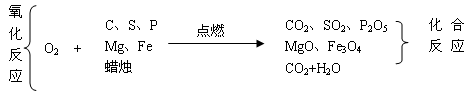
氧气是一种化学性质比较活泼的气体。